A recente notícia de que o ator Sam Neill alcançou a remissão de um câncer em estágio três após participar de um ensaio clínico de terapia CAR T-cell em Sydney trouxe um novo fôlego ao debate sobre a próxima geração de tratamentos oncológicos. O caso, amplamente divulgado, serve como uma vitrine para uma tecnologia que, embora ainda em fase de amadurecimento, começa a demonstrar resultados clínicos robustos em pacientes que esgotaram as opções terapêuticas convencionais.
Segundo especialistas do Walter and Eliza Hall Institute of Medical Research, a terapia não deve ser encarada como um milagre, mas como o ápice da aplicação prática da imunologia moderna. O tratamento funciona ao reprogramar geneticamente as células T do próprio paciente, capacitando o sistema imunológico a identificar e atacar células cancerígenas com uma precisão que a quimioterapia tradicional raramente alcança. A remissão de Neill, descrita pelo próprio ator como "ciência em sua melhor forma" (em tradução livre), ilustra a mudança de paradigma que a medicina de precisão promete consolidar na próxima década.
A mecânica da revolução imunológica
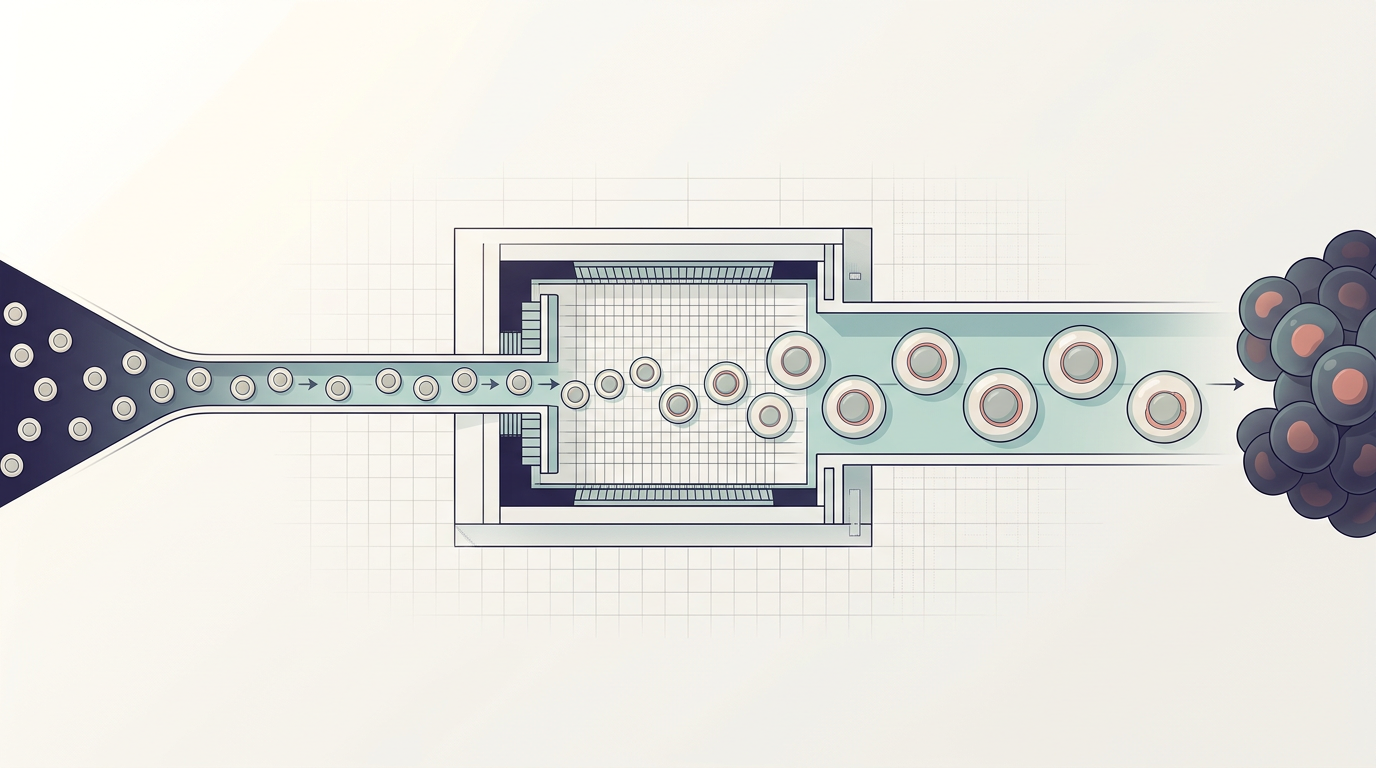
A terapia CAR T-cell, sigla para Receptor de Antígeno Quimérico, atua por meio de engenharia celular ex vivo. O processo começa com a coleta de células T do sangue do paciente, que são então enviadas a um laboratório especializado. Ali, essas células passam por uma modificação genética para expressar receptores específicos capazes de reconhecer proteínas presentes na superfície das células tumorais. Uma vez reinfundidas no paciente, essas células atuam como um exército customizado, capaz de buscar e destruir a malignidade de forma persistente.
Historicamente, o tratamento enfrentou desafios significativos, desde a complexidade logística da fabricação personalizada até efeitos colaterais severos, como a síndrome de liberação de citocinas. No entanto, o aprimoramento dos protocolos clínicos e o melhor manejo dessas respostas imunes têm permitido que mais pacientes tolerem o procedimento. O que antes era restrito a cenários de desespero absoluto começa a ser estudado para aplicações mais amplas, sugerindo que a fronteira do possível na oncologia está sendo redefinida pela capacidade de reprogramar células do próprio hospedeiro.
Desafios estruturais e barreiras de custo
Apesar do entusiasmo científico, a viabilidade da terapia CAR T-cell em larga escala permanece como um dos maiores gargalos da medicina contemporânea. O processo de produção é inerentemente caro e exige infraestrutura laboratorial de ponta, o que torna o custo por paciente proibitivo para a maioria dos sistemas públicos de saúde ao redor do mundo. A personalização extrema, embora seja a chave para a eficácia, é também o principal obstáculo para a democratização do tratamento.
Além disso, a cadeia de suprimentos para a fabricação dessas células é complexa. A necessidade de manter a viabilidade biológica durante o transporte e o processamento exige uma logística que poucas instituições conseguem prover com consistência. Para o mercado, o desafio reside em transitar de um modelo de nicho para uma plataforma escalável. A pressão por inovações que simplifiquem a produção — ou que permitam o uso de células de doadores saudáveis, as chamadas terapias alogênicas — é intensa, pois é apenas através da redução de custos que a técnica deixará de ser uma exceção para se tornar uma norma clínica.
Implicações para o ecossistema de saúde
Para reguladores e gestores de saúde, a ascensão das terapias gênicas coloca em xeque os modelos tradicionais de reembolso e precificação de medicamentos. Diferente de uma pílula que é tomada diariamente, a CAR T-cell é muitas vezes um tratamento único, o que exige novas métricas de valor e financiamento de longo prazo. O setor de biotecnologia observa atentamente como os governos vão equilibrar o incentivo à inovação com a necessidade de garantir que pacientes não sejam excluídos por critérios puramente econômicos.
No Brasil, onde o sistema público de saúde possui capilaridade única, a adoção de tecnologias tão avançadas demanda uma transição cuidadosa. A colaboração entre institutos de pesquisa nacionais e centros globais de biotecnologia será fundamental para que o país não apenas consuma, mas participe do desenvolvimento dessa nova onda de tratamentos. A questão não é apenas se a ciência funciona, mas se a infraestrutura hospitalar e regulatória está preparada para absorver essa mudança sem colapsar sob o peso dos custos operacionais.
Perspectivas e o horizonte clínico
O que permanece incerto é a duração da eficácia a longo prazo para uma gama mais vasta de tumores sólidos, que apresentam microambientes muito mais hostis do que as neoplasias hematológicas onde a técnica teve sucesso inicial. A comunidade científica continua a investigar como contornar os mecanismos de resistência que os tumores desenvolvem para escapar da vigilância imunológica.
O sucesso observado em casos de alto perfil como o de Sam Neill acelera o investimento em pesquisa e atrai o capital necessário para os próximos saltos tecnológicos. O que observaremos nos próximos anos será uma corrida para tornar esses procedimentos mais seguros, rápidos e, fundamentalmente, acessíveis. A ciência, embora tenha apenas arranhado a superfície, demonstrou que a imunoterapia deixou de ser uma promessa teórica para se tornar uma realidade transformadora na prática clínica.
O avanço da terapia CAR T-cell nos força a repensar a própria definição de tratamento oncológico. À medida que a tecnologia se torna mais refinada, a medicina se afasta da era da destruição indiscriminada de células, típica da quimioterapia, para entrar em uma fase de precisão biológica. A transição não será linear, nem barata, mas o precedente estabelecido pela remissão clínica sugere que o custo da inação pode ser, em última análise, muito superior ao investimento necessário para escalar a inovação.
Com reportagem de The Guardian Science
Source · The Guardian Science